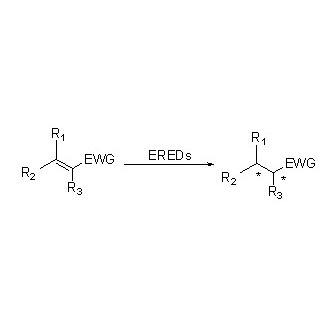
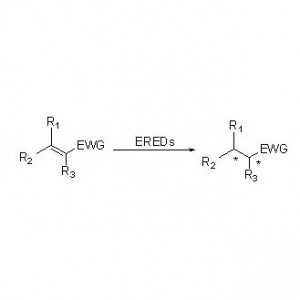
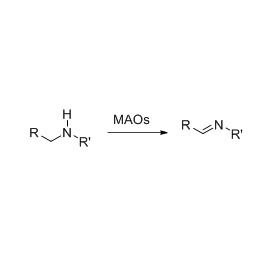
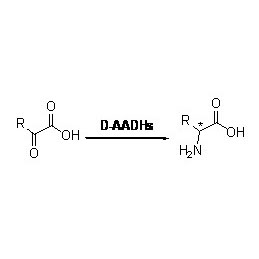
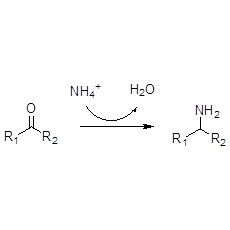
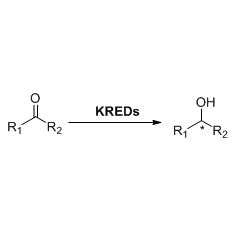
Ene reductasa (ERED)
Las ES-ERED catalizan diversos tipos de sustratos debido a su amplio espectro de sustratos. En general, los enlaces C=C de los compuestos α, β -insaturados con grupos que absorben electrones (incluidos cetonas, aldehídos, grupos nitro, ácidos carboxílicos, ésteres, anhídridos, lactonas, iminas, etc.) se reducen fácilmente mediante las ES-ERED, pero los dobles enlaces no activados no.
SyncoZymes ha desarrollado 46 tipos de productos enzimáticos ERED (numerados como ES-ERED-101~ES-ERED-146).
Mecanismo catalítico:
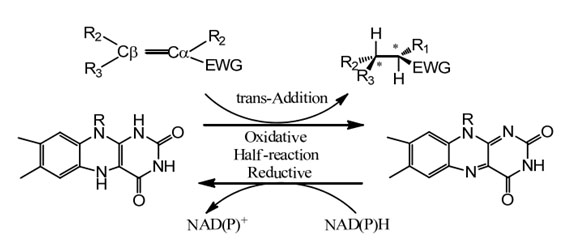
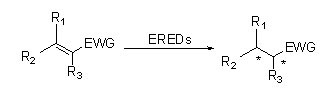
| Enzimas | Código de producto | Especificación |
| Polvo de enzimas | ES-ERED-101~ ES-ERED-146 | un conjunto de 46 Ene Reductasas, 50 mg cada una 46 artículos * 50 mg / artículo, u otra cantidad |
| Kit de cribado (SynKit) | ES-ERED-4600 | un conjunto de 46 Ene Reductasas, 50 mg cada una 46 artículos * 50 mg / artículo, u otra cantidad |
★ Alta especificidad de sustrato.
★ Fuerte selectividad quiral.
★ Alta tasa de conversión.
★ Menos subproductos.
★ Condiciones de reacción suaves.
★ Respetuoso con el medio ambiente.
★ Alta seguridad.
➢ Normalmente, el sistema de reacción debe incluir sustrato, solución tampón (pH óptimo de reacción), coenzimas (NAD(H) o NADP(H) ), sistema de regeneración de coenzimas (por ejemplo, glucosa y glucosa deshidrogenasa) y ES-ERED.
➢ Todos los ES-ERED se pueden probar respectivamente en el sistema de reacción anterior o con el kit de detección ERED (SynKit ERED).
➢ Todos los tipos de ES-ERED correspondientes a diversas condiciones de reacción óptimas deben estudiarse individualmente.
➢ Las altas concentraciones de sustrato o producto pueden inhibir la actividad de ES-ERED. Sin embargo, esta inhibición puede revertirse mediante la adición de sustrato por lotes.
Ejemplo 1 (aldehídos o cetonas α,β-insaturados)(1):
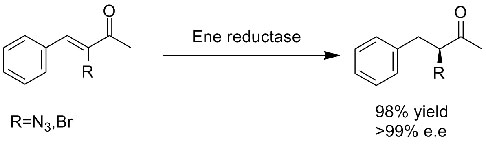
Ejemplo 2 (ácidos carboxílicos α,β-insaturados y sus derivados)(2):
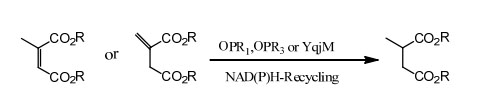
Mantener durante 2 años por debajo de -20℃.
Nunca exponer a condiciones extremas como: altas temperaturas, pH alto/bajo y disolventes orgánicos de alta concentración.
1. Lucidio C, Fardelone J, Augusto R, et tal. J.Mol.Catal.B:Enzym., 2004, 29: 41-45.
2. Stueckler C, Hall M, Ehammer H, et al. .Org.Lett, 2007, 9(26): 5409-5411.